leyu乐鱼体育-3个中药创新药获批上市!9款贝伐珠单抗同台竞技,百济神州、方盛制药、天士力……
 举世医药网 > 医药资讯 > 行业新闻 > 正文 3个中药立异药获批上市!9款贝伐珠单抗同台竞技,百济神州、方盛制药、天士力……2021/12/7 来历:药智网 浏览数:
举世医药网 > 医药资讯 > 行业新闻 > 正文 3个中药立异药获批上市!9款贝伐珠单抗同台竞技,百济神州、方盛制药、天士力……2021/12/7 来历:药智网 浏览数:
中药立异药迎来收成期,玄七健骨片、芪蛭益肾胶囊、坤心宁颗粒3款中药立异药的上市注册申请获NMPA核准;生物近似药竞争剧烈,贝达药业、东曜药业和复宏汉霖的贝伐珠单抗接踵获批;百济神州罕有病新药在中国正式获批;先声药业引进CDK4/6按捺剂提交上市申请,更多动态以下:
国内审评审批·新动态
本周CDE有70个受理号(4leyu��������5个品种)报出产打点状况更新,此中海正生物/贝达药业、东曜药业、复宏汉霖的贝伐珠单抗打针液,百济神州的打针用司妥昔单抗,方盛制药的玄七健骨片、凤凰制药的芪蛭益肾胶囊和天士力的坤心宁颗粒备受存眷,更多动态以下:
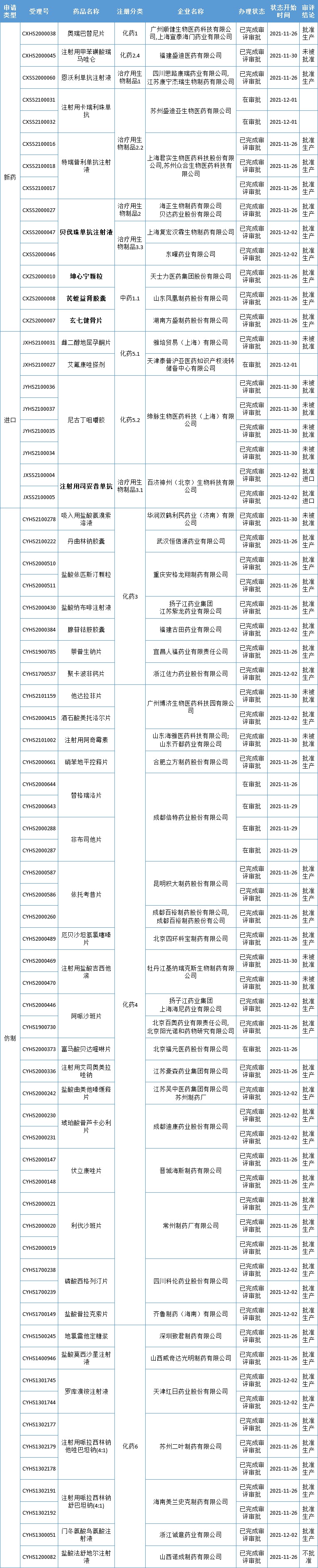
数据来历:药智数据
3个中药立异药获批上市!
继月初,康缘药业的中药立异药银翘清热片获批上市后,本周,国度药监局又核准了3款1类中药新药,包罗方盛制药的玄七健骨片、凤凰制药的芪蛭益肾胶囊和天士力的坤心宁颗粒。
国度药监局暗示,上述3款中药立异药均是基在中医临床经验方根本上研制,经由过程展开随机、双盲、抚慰剂平行对比、多中间临床实验,取得平安性、有用性证据,核准上市后将为临床相干疾病的患者供给新的医治选择。
2021年截至今朝,国度药监局在告急核准清肺排毒颗粒、化湿败毒颗粒、宣肺败毒颗粒的根本上,又核准了6个中药新药上市。
玄七健骨片
该药上市许可持有报酬湖南边盛制药股分有限公司,其临床实验研究成果显示可用在轻中度膝骨关节炎中医辨证属筋脉瘀滞证的医治。
方盛制药采纳“中药、化药、生物药”三药并举计谋。此中在中药范畴,方盛制药已成功开辟"欣雪安"牌心脑血管科、"金蓓贝"牌儿科、"方盛堂"牌骨伤科等几年夜系列产物。
芪蛭益肾胶囊
该药上市许可持有报酬山东凤凰制药股分有限公司,其临床实验研究成果显示可用在初期糖尿病肾病气阴两虚证的医治。
最近几年来,凤凰制药开辟出了具有自立常识产权的国度三类中药新药天丹通络胶囊、复方川芎胶囊、金石清热颗粒、女珍颗粒等立异药物。正在研发中药项目有芪黄胶囊。
坤心宁颗粒
坤心宁颗粒曾用名为坤怡宁颗粒,上市许可持有报酬天士力医药团体股分有限公司,其临床实验研究成果显示可用在女性更年期综合征中医辨证属肾阴阳两虚证的医治。
3款贝伐珠单抗生物近似药获批上市
药智数据显示,本周有3款贝伐珠单抗生物近似药获批上市,来自海正生物/贝达药业、东曜药业、复宏汉霖。
贝伐珠单抗是一款抗血管内皮细胞发展因子单克隆抗体(抗VEGF mAb)。原研安维汀2004年2月初次获FDA核准上市,今朝已在全球已获批多个顺应症,在我国获批6个顺应症,别离是:转移性结直肠癌(mCRC)、非小细胞肺癌(NSCLC)、胶质母细胞瘤(GBM)、肝细胞癌(HCC)、卵巢癌(OC)、宫颈癌(CC)。
药智数据显示,除罗氏的贝伐珠单抗原研外,还8款贝伐珠单抗生物近似药在中国获批上市,别离是齐鲁制药、信达生物、恒瑞医药、博安生物、百奥泰、海正生物/贝达生物、东曜药业和复宏汉霖。另外,正年夜晴和也已递交上市申请。
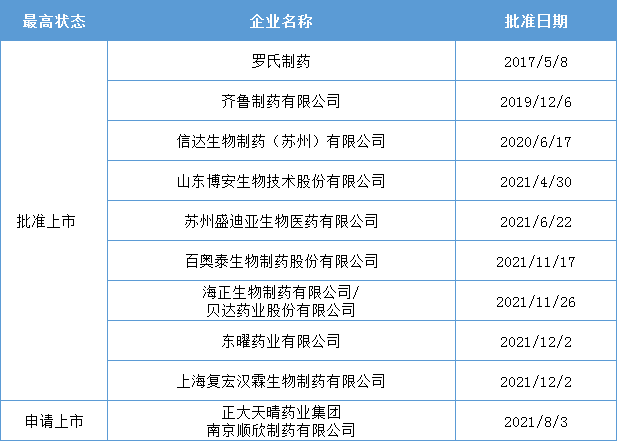
数据来历:药智数据
海正生物/贝达药业申报的贝伐珠单抗打针液MIL60获批顺应症为:转移性结直肠癌和晚期、转移性或复发性非小细胞肺癌。2017年2月,贝达药业与北京天广实生物手艺股分有限公司就贝伐珠单抗打针液项目告竣合作,受托出产企业为博锐生物部属子公司海正生物制药有限公司。
东曜药业发申报的贝伐珠单抗打针液TAB008获批顺应症为:医治晚期、转移性或复发性非鳞状非小细胞肺癌和转移性结直肠癌。这是是东曜药业首个获批上市的抗体药。
复宏汉霖申报的贝伐珠单抗生物近似药HLX04获批顺应症为:晚期、转移性或复发性非小细胞肺癌和转移性结直肠癌患者的医治。据悉,复宏汉霖还与亿胜生物签定全球许可和谈,配合开辟HLX04眼科顺应症,合作金额超4300万美元。
百济神州引进的罕有病新药「司妥昔单抗」正式获批
12月2日,国度药品监视治理局经由过程优先审评审批法式核准临床急需罕有病药品打针用司妥昔单抗(英文名: Siltuximab for Injection)的进口注册申请,用在人体免疫缺点病毒(HIV)阴性和人疱疹病毒8型(HHV-8)阴性的多中间卡斯特曼病(MCD)成人患者。
司妥昔单抗是一种人-鼠嵌合单克隆抗体,可阻断人白细胞介素-6(IL-6)与IL-6受体相连系,对IL-6发生按捺感化,继而按捺细胞发展。该品种的上市为患者供给了医治选择。司妥昔单抗自2014年初次获批以来,已在全球40多个国度和地域取得核准用在医治人类免疫缺点病毒(HIV)阴性、人类疱疹病毒8(HHV-8)阴性的多中间型Castleman病患者。
在中国,司妥昔单抗曾因罕有病用药被纳入《第一批临床急需境外新药》名单。
2020年1月,百济神州与EUSA Pharma告竣合作,取得了司妥昔单抗和别的一款抗体药物在年夜中华地域开辟和贸易化权力。另外一款药物为达妥昔单抗β(dinutuximab beta),已在本年8月在中国获批上市,用在医治12月龄和以上的高危神经母细胞瘤患者。
国内审评审批·新受理
本周CDE新增报出产受理号43个,共29个品种,此中先声药业的打针用曲拉西利备受存眷,更多动态见下表:
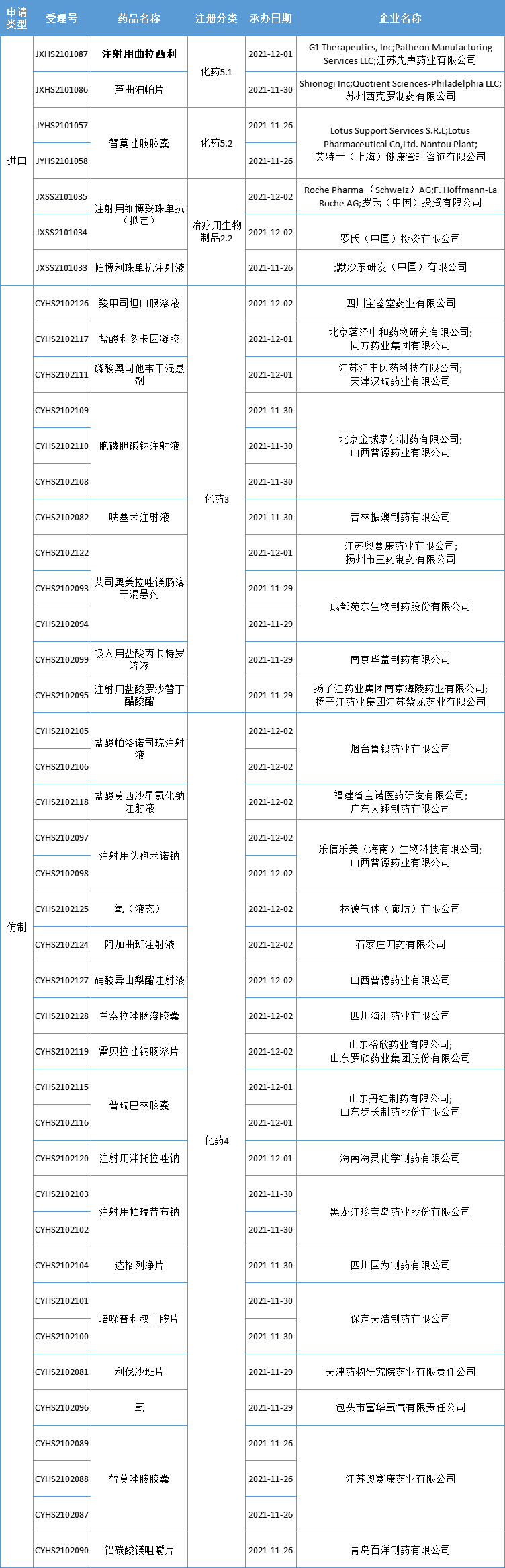
数据来历:药智数据
先声药业引进CDK4/6按捺剂「曲拉西利」上市申请获受理
近日,先声药业向国度药品监视治理局递交的骨髓庇护立异药打针用曲拉西利(Trilaciclib)上市许可申请(NDA)获受理,本次申请顺应症为:在接管含铂类药物结合依托泊苷方案的普遍期小细胞肺癌患者中预防性利用,以下降化疗引发的骨髓按捺的产生率。
曲拉西利是G1 Therapeutics公司开辟的一款短效CDK 4/6按捺剂,曾被美国FDA授与冲破性医治认定和优先审评资历。该药已在本年2月在美国上市,用在下降普遍期小细胞肺癌患者在接管某些类型化疗时呈现的骨髓按捺频率。
除小细胞肺癌外,G1公司还启动了曲拉西利在三阴性乳腺癌和转移性结直肠癌(mCRC)的Ⅲ期临床实验,关在乳腺癌新辅助化疗、非小细胞肺癌二线医治和膀胱癌一线医治的摸索性研究也在境外进行中。
2020年8月,G1公司与先声药业告竣达1.7亿美元的独家许可和谈,先声药业取得这款立异疗法在年夜中华地域所有顺应症的开辟和贸易化权益。今朝正在展开曲拉西利在小细胞肺癌、结直肠癌、三阴性乳腺癌三项顺应症的III期临床实验。
编纂:Rae上一篇:leyu乐鱼体育-2021版基药目录管理办法出炉!新增“儿童药品目录”,调整依据6大因素…… 下一篇:leyu乐鱼体育-恒瑞医药、再鼎医药、丽珠集团等达成新药授权合作
